|
Redacción
La Administración de Alimentos y Fármacos estadounidense (FDA) ha otorgado a Boston Scientific la aprobación regulatoria de su sistema S-ICD®, el primer y único desfibrilador implantable subcutáneo (S-ICD) disponible en el mercado para el tratamiento de los pacientes expuestos a sufrir una muerte súbita. El sistema S-ICD se implanta debajo de la piel, sin necesidad de introducir en el corazón los cables finos y aislados conocidos como electrodos. De este modo, no se toca el corazón ni los vasos sanguíneos, lo que constituye una alternativa a los desfibriladores automáticos implantables (DAI), que requieren la colocación de electrodos en el corazón. El Dr. Raul Weiss, catedrático de Medicina Cardiovascular en la Ohio State University, ha explicado que “el sistema S-ICD establece la primera nueva categoría de dispositivos para el control del ritmo cardiaco desde la aparición de la terapia de resincronización cardiaca. Ahora los médicos disponen de una opción terapéutica revolucionaria que protege a los pacientes de la muerte súbita sin necesidad de tocar el corazón”.
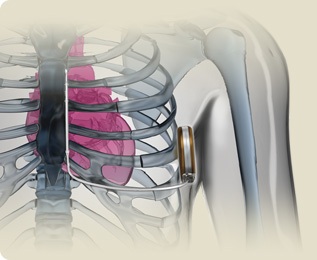
Imagen del sistema S-ICD® de Boston Scientific.
|
La aprobación del sistema S-ICD ha tomado como base los datos obtenidos de un estudio clínico prospectivo, no aleatorizado, multicéntrico, con 330 pacientes, en el que se evaluó la seguridad y la efectividad del sistema en pacientes que presentaban riesgo de muerte súbita. El sistema S-ICD alcanzó los criterios de valoración principales del estudio y los resultados han sido presentados este año en las sesiones científicas anuales de la Heart Rhythm Society. Dichos resultados avalan el sistema S-ICD como una nueva opción terapéutica importante para una amplia variedad de pacientes en prevención primaria y secundaria.
Por su parte, Hank Kucheman, director general de Boston Scientific, ha destacado que “con la adición del sistema S-ICD, Boston Scientific cuenta con una cartera sólida y altamente diferenciada de productos, que ayudará a impulsar nuestra estrategia de crecimiento”. “Somos la única empresa que ofrece un desfibrilador implantable subcutáneo aprobado por la FDA, y es de esperar que sigamos siéndolo durante varios años. El sistema S-ICD, junto con la numerosas aprobaciones regulatorias que hemos recibido recientemente y con nuestros otros productos innovadores, como el dispositivo WATCHMAN para el cierre de la orejuela auricular izquierda y el sistema de termoplastia bronquial Alair®, demuestra nuestro compromiso permanente con el desarrollo y la presentación de productos innovadores para médicos y pacientes”.
Datos recientes indican que unas 850.000 personas en EEUU presentan riesgo de sufrir una muerte súbita, por lo que tendrían indicado un DAI, pero, sin embargo, aún no han recibido esta protección. El Dr. William T. Abraham, miembro del American College of Cardiology y director de la División de Medicina Cardiovascular del Ohio State University Heart Center, ha indicado que “cada año miles de pacientes para quienes estaría indicado un DAI no son derivados a un especialista, y no reciben tratamiento. El sistema S-ICD es una nueva opción terapéutica importante que tiene el potencial de mejorar la aceptación de los pacientes hacia el tratamiento con DAI”.
Generador de impulsos y electrodo, sus componentes principales
El sistema S-ICD está diseñado para ofrecer la misma protección frente a la muerte súbita que los DAI transvenosos. El sistema cuenta con dos componentes principales: el generador de impulsos, que suministra energía al sistema, monitoriza la actividad cardiaca y realiza las descargas necesarias, y el electrodo, que permite al dispositivo percibir el ritmo cardiaco y producir descargas cuando es necesario. Ambos componentes se implantan debajo de la piel, el generador a un costado del tórax y el electrodo al lado del esternón. A diferencia de lo que sucede con los DAI transvenosos, no es necesario tocar el corazón ni los vasos sanguíneos. El implante del sistema S-ICD es sencillo y se guía por puntos anatómicos, sin necesidad de fluoroscopia, una técnica que sí es necesaria para el implante de los electrodos acoplados a los sistemas de DAI transvenosos.
Boston Scientific tiene previsto comenzar una comercialización escalonada del S-ICD, con una expansión paulatina a medida que los profesionales médicos reciban la formación necesaria en el uso seguro y eficaz del sistema. La empresa ha adquirido el sistema S-ICD este año, tras comprar la empresa Cameron Health, Inc. El sistema S-ICD recibió el marcado CE en 2009 y está comercializado en numerosos países europeos, así como en Nueva Zelanda. Hasta la fecha se han implantado más de 1.400 dispositivos a pacientes en todo el mundo.
El sistema S-ICD tiene como objetivo ofrecer una terapia de desfibrilación para el tratamiento de taquiarritmias potencialmente mortales en pacientes que no presentan bradicardia sintomática, taquicardia ventricular incesante o taquicardia ventricular espontánea y frecuentemente recurrente, que se resuelven de forma fiable mediante estimulación antitaquicárdica. El dispositivo WATCHMAN es un dispositivo en fase de investigación en los EE.UU. En virtud de las leyes vigentes, su uso está limitado al contexto de la investigación y no se encuentra disponible en el mercado.
|


